의약품특허출원, 임상 전에도 가능할까?|실험 데이터 준비 기준 총정리
🔎 핵심 요약
- 의약품특허출원은 임상 전에도 가능 (단, 조건 충족 시)
- 핵심은 약리 효과를 입증하는 실험 데이터
- 세포(In-vitro) 또는 동물(In-vivo) 실험 결과가 중요
- 단순 주장 ❌ → 수치 데이터 + 기전 설명 필수
👉 결론: 임상 전이라도 데이터 구조 설계가 되어 있다면 충분히 권리 확보 가능
의약품특허출원, 임상 전에 해도 괜찮을까?
많은 연구자와 바이오 스타트업이 고민하는 질문입니다.
“임상 1상도 안 했는데 특허 출원이 가능할까?”
결론부터 말하면 가능합니다.
하지만 다음 조건이 반드시 필요합니다.
👉 약리 효과가 객관적으로 입증되어야 함
단순히
- “항암 효과 있음”
- “치료 가능성 있음”
이 정도로는 부족합니다.
✔ 인정되는 기준
- 세포 실험(In-vitro) 결과
- 동물 실험(In-vivo) 결과
- 통계적으로 유의미한 수치 데이터
즉, 임상 데이터는 필수는 아니지만
👉 효과 입증 데이터는 필수입니다
1. 왜 임상 전에 출원하는 것이 중요한가
의약품 분야는 “타이밍”이 매우 중요합니다.
너무 늦으면
→ 논문 발표, 학회 공개 등으로 신규성 상실
너무 빠르면
→ 데이터 부족으로 기재 불비 또는 진보성 부족
그래서 가장 전략적인 시점은 다음입니다.
✔ 추천 시점
👉 비임상 데이터 확보 직후 (골든타임)
- 효능 입증 완료
- 데이터 확보 상태
- 아직 외부 공개 전
이 시점이 가장 이상적입니다.
2. 의약품특허출원 실험 데이터 기준 (심사관 관점)
심사관은 다음 3가지를 중심으로 판단합니다.
① 약리 기전 (Mechanism of Action)
- 물질이 어떻게 작용하는지 설명 필요
- 단순 결과가 아니라 작용 원리까지 제시
② 수치 기반 실험 데이터
- Dose-response (투여량 대비 반응)
- IC50, EC50 등 정량 지표
- 그래프, 표 형태 필수
👉 핵심
“숫자로 설명되지 않으면 인정받기 어렵다”
③ 비교우위 (대조군 대비 효과)
- 기존 치료제 대비 개선 여부
- 효능 증가 / 독성 감소
👉 진보성 판단 핵심 요소
📌 한 줄 정리
👉 데이터의 양이 아니라 ‘설득력 있는 구조’가 중요
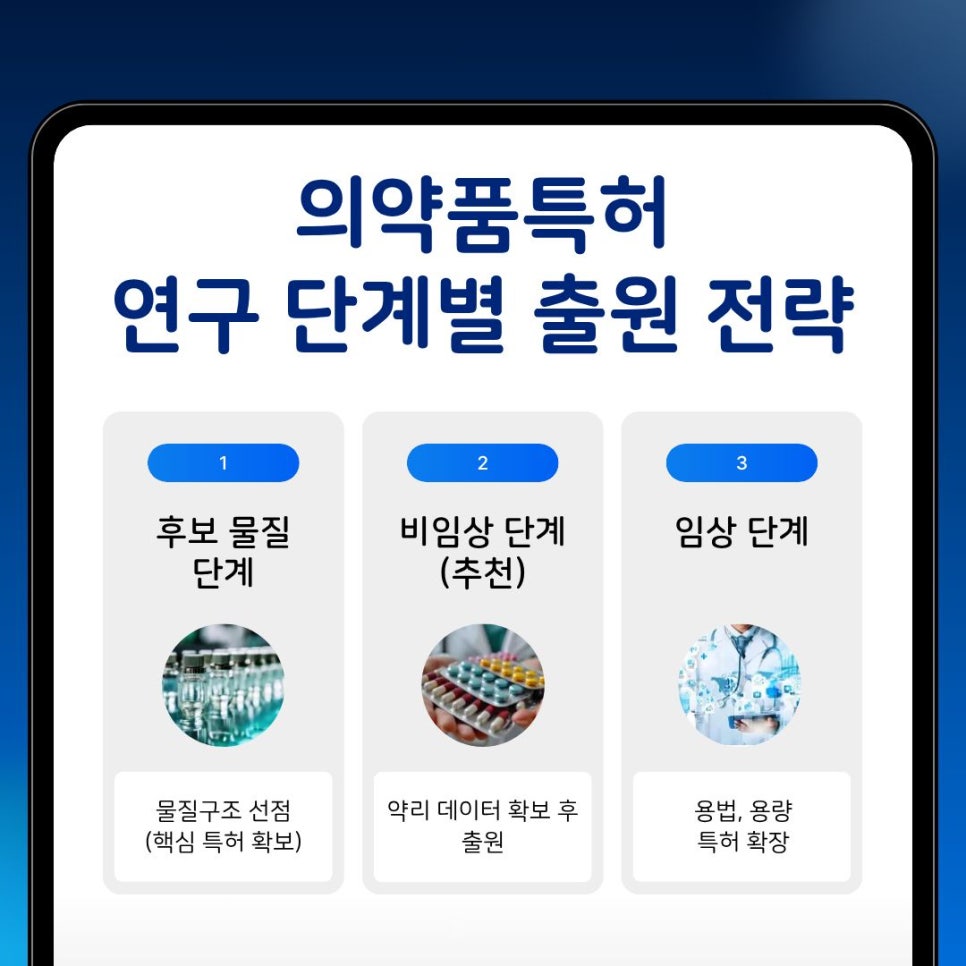
3. 연구 단계별 출원 전략 (실무 기준)
의약품특허는 단계별 전략이 다릅니다.
✔ 후보물질 단계
- 물질특허 선점
- 가장 강력한 권리 확보
✔ 비임상 단계 (추천)
- 약리 데이터 확보 후 출원
- 가장 안정적인 등록 가능 구간
✔ 임상 단계
- 용법·용량 특허 확장
- 제형, 병용투여 전략 추가
👉 핵심
하나의 특허가 아니라 ‘포트폴리오’로 확장해야 함
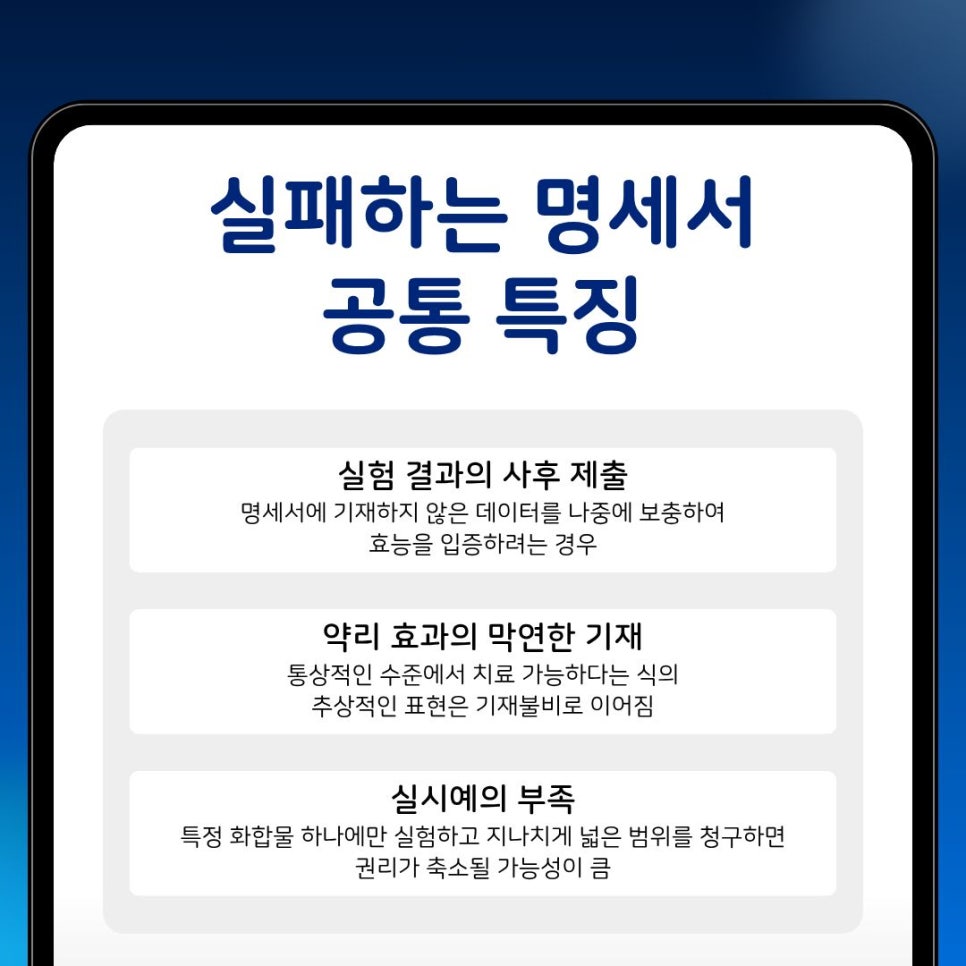
4. 실패하는 의약품 특허의 공통 특징
실무에서 반복되는 실패 패턴입니다.
❌ 출원 후 데이터 추가
→ 의약 분야에서는 거의 인정되지 않음
❌ 효과를 추상적으로 표현
→ “효과 있음” 수준 → 기재 불비
❌ 실시예 부족
→ 한 개 실험으로 넓은 범위 청구
→ 권리 축소 또는 거절
👉 핵심
출원 시점에 이미 완성된 구조가 필요
5. 최신 심사 트렌드 (2026 기준)
최근 심사 경향은 “개량 특허”의 가치 상승입니다.
✔ 용법·용량
- 복용 주기 개선
- 투여 방식 변화
✔ DDS (Drug Delivery System)
- 특정 부위 전달 기술
- 부작용 감소
✔ 병용 투여
- 시너지 효과 입증
👉 포인트
물질이 아니라 ‘사용 방식’도 강력한 특허가 된다
6. 의약품특허출원 체크리스트 (실무용)
출원 전 반드시 확인해야 합니다.
- 약리 기전 설명 가능 여부
- 수치 기반 실험 데이터 확보
- 대조군 비교 데이터 존재
- 실시예 2개 이상 구성
- 확장 가능한 청구항 구조 설계
👉 하나라도 부족하면
“출원”보다 “데이터 보강”이 우선입니다
마무리
의약품특허출원은 단순한 출원이 아닙니다.
👉 데이터 + 타이밍 + 구조 설계의 싸움
- 늦으면 신규성 상실
- 빠르면 데이터 부족
결국 핵심은 하나입니다.
👉 “지금 데이터로 설득 가능한가”
이 판단만 정확히 해도
등록 가능성은 크게 달라집니다.
📞 대표 번호 : [1566-7190]
✉️ 문의: [기율특허법인 1:1 상담 바로가기]
특허청 홈페이지 [바로가기]